中科院发现α-疱疹病毒蛋白与DNA相分离聚集地
然而,人们还没有发现任何病原蛋白通过干预cGAS-DNA相分离来抑制cGAS-STING通路。总体而言,病原微生物对宿主细胞相分离的干预和调控,也鲜有研究报道。而且,病毒间质蛋白对cGAS-DNA相分离的抑制,代表了一种全新的病原—宿主互作机制。
cGAS-STING通路可以识别细胞质中异常出现的DNA(病原体感染引入的外源DNA或宿主异常释放的内源DNA)并诱导I型干扰素和其他促炎因子的表达。 作为广谱细胞质DNA受体,cGAS识别DNA无序列特异性,因此该途径可以响应多种病原感染。 然而,尚未发现致病蛋白通过干扰 cGAS-DNA 相分离来抑制 cGAS-STING 途径。 总体而言,关于病原微生物对宿主细胞相分离的干扰和调控的研究报道较少。
这次,研究人员发现以ORF52(γ-疱疹病毒编码)和VP22(α-疱疹病毒编码)为代表的一类病毒间质蛋白可以干扰和破坏cGAS-DNA的自然免疫相分离,从而抑制宿主细胞先天免疫反应。 研究结果表明,ORF52/VP22型病毒间质蛋白在体外和细胞内均能有效抑制cGAS-DNA相分离。
而且,病毒颗粒携带的大量ORF52可以在病毒感染早期作用于cGAS-DNA相分离。 研究人员表示,病毒蛋白对cGAS-DNA相分离的抑制作用并不取决于病毒蛋白与cGAS之间的直接相互作用,而是取决于病毒蛋白被DNA诱导形成自身相分离的能力。 病毒蛋白和DNA的相分离和聚集取决于它们的多价相互作用而不是简单的亲和力。
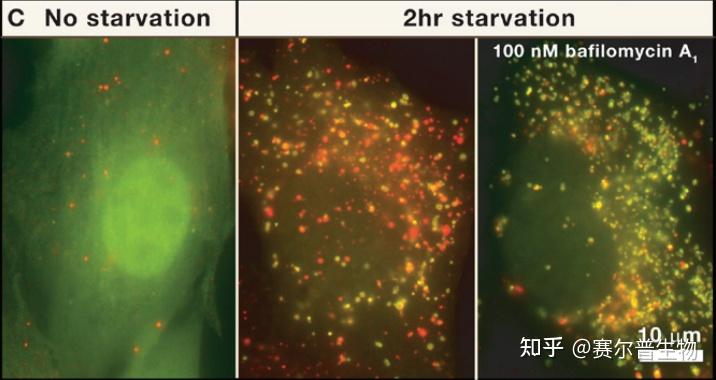
研究人员还发现免疫逃逸,削弱病毒蛋白与DNA相分离的能力免疫逃逸,会直接降低其抑制cGAS-DNA相分离以及整个通路的能力。 此外,病毒间质蛋白对cGAS-DNA相分离的抑制代表了一种新的病原体-宿主相互作用机制。
相关论文信息:
很赞哦 ()
- 上一篇: 月经期可以喝红酒木瓜汤吗?红酒会影响经期吗
- 下一篇: 备孕期间男人吃什么补精补肾的中成药应该如何选择