62基金项目国家自然科学基金资助项目(3,)
62基金项目国家自然科学基金捐助项目(3,女,硕士生,专业方向神经及血管电生理。通信作者652),男,院士,从事神经及血管电生理研究。第252007年10昌吉学院学报(自然科学版)()Vol2007文章编号:(2007)山西地方与民族高发病教育部重点实验室,内蒙呼和浩特云南昆明)摘要:目的构建胎鼠背根神经节(root,DRG)神经元原代培养的方式。方式无菌条件下取E16胎鼠DRG进行原代培养,观察神经元生长状态并用神经元特异性烯醇化酶(,NSE)免疫细胞物理染色鉴别细胞。结果培养的DRG神经元可存活1个月左右,并长出凸出,产生密集的网路。NSE鉴别细胞阳性抒发率高,神经元达到90%左右含量。推论本文构建了DRG神经元细胞简约、经济、高效的培养方式并成功鉴定了神经元。为对神经元的深入研究提供了实验模型。关键词:神经元;细胞培养;背根神经节;特异性烯醇化酶;免疫细胞物理中图分类号:R338.细胞培养是从体内组织取出细胞在体外模拟体内环境下,使其生长繁育,并维持其结构和功能的一种培养技术。
该技术早已成为现今生物医学研究的主要方式之一。其主要优点在于,体外细胞培养的条件降低了在体神经组织的复杂性以及对细胞环境的操纵性,有利于预测和研究单个细胞在在体的功。据悉,有大量证据表明,体外培养的神经细胞也能抒发许多在体细胞的同样特点,更重要的是培养的细胞的膜特点不变,受体的所有组成成份不。并且神经元高度分化,离体和出生后即不再分裂,所需营养条件较高,所以对神经元进行体外分离培养比较困难。本实验致力完善胚胎小鼠背根神经节神经元原代培养方式,为轴突生长、信号转导、神经营养因子等神经生物学的研究和电生理学研究(尤其是膜片钳这类对膜结构要求比较高的电生理研究)提供单个神经元模型。实验植物选用健康成年雄雌SD小鼠,由山西地方病研究所植物繁殖中心提供,孕鼠的确定依据植物交配后次晨肛门见到阴栓为妊娠第1d神经元特异性烯醇化酶英文,妊娠第16d药品与仪器多聚赖谷氨酸(PLL)、谷氨丙酯、、PBS片剂均为Sigma公司片产品,DMEM培养基为Gibco公司产品,胎牛血浆为美国公司产品,兔抗鼠神经元特异性烯醇化酶(NSE)、S2ABC试剂盒、TAB染色试剂盒均为博士德公司产品,倒置相差显微镜为公司产品。
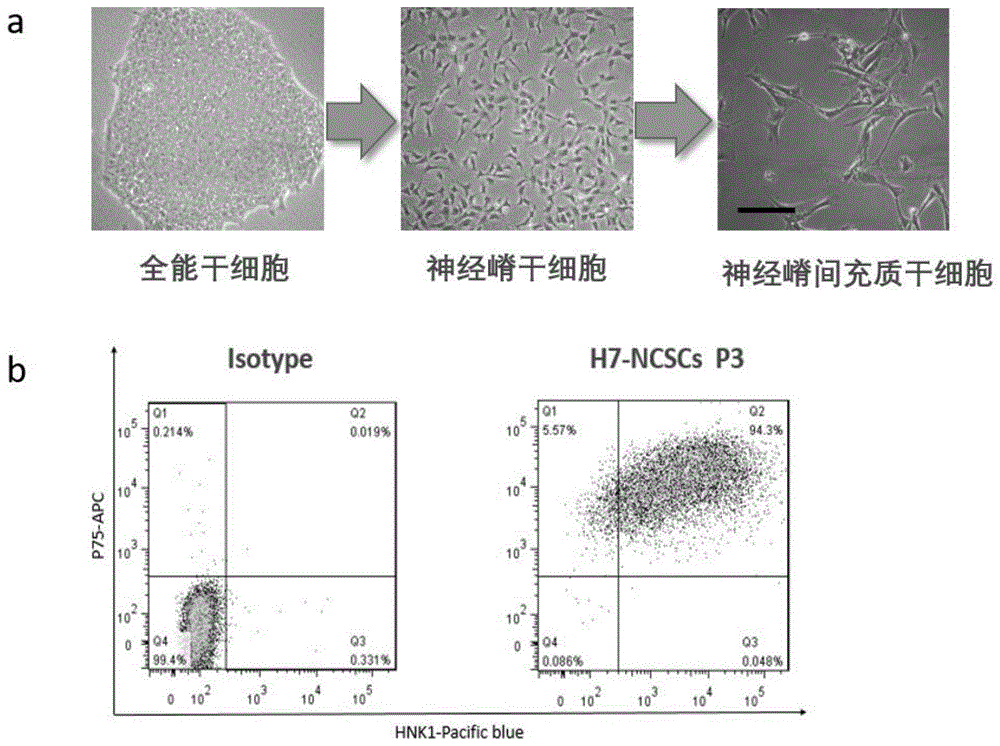
培养前的打算将无菌的2424mm玻璃盖片装入35mm培养多聚赖谷氨酸37培养箱中包被过夜,PBS冲洗3遍后,超净台北紫外灯照射45min。脑干背根神经节的取材与培养将E16孕鼠乙腈麻醉后无菌取其胚胎,装入PBS液中,迅速剪开腹部皮肤及骨膜,取出脊柱,纵行剥开,依次在3个盛有PBS次以后倒入10%FBS的DMEM培养基中,在解剖显微镜下曝露椎管和椎间孔神经元特异性烯醇化酶英文,可见两旁胸椎的两侧隐窝中有方形无瑕的脊神经节,用显微镊挨个切除神经节,并尽量剥除神经节表面的骨膜,装入35mm培养皿中,外科剪将神经节剪至1mm大小的尸块后移入2mL25%混和消化液的离心管中,4冰柜中作用20min后,在37CO2培养箱中消化20min,吸去消化液,直接加入含100100219FBS的DMEM培养基中止消化反应,离心后弃上清,用DMEM培养基重悬细胞,将其制成单细胞悬液,以10mL的密度接种于用多聚赖谷氨酸包被处理的35mm培养皿中,于37CO2培养箱中进行培养。每周换液2细胞形态观察将培养不同时间生长状态下的神经元于倒置相差显微镜下进行形态学观察,观察其形态及生长状态。
免疫细胞物理染色取培养7d后的神经元,吸出培养液上清,4聚甲醛4下固定40minPBS清洗3温度下加入绵羊血浆封闭液作用20min,吸出封闭液,不冲洗。加入1200的兔抗鼠神经元特异性烯醇化酶,4过夜,0.01mol/PBS清洗3次。加入生物素化绵羊抗兔IgG,37PBS清洗3次,每次5min。使用DAB显色试剂盒,取1mL分馏水,加试剂盒中A、B、C试剂各1滴,混匀后按50nL/孔加入培养板,温度下显色,镜下控制反应时间,分馏水漂洗。苏木精复染,自来水冲洗。酸酒精分化几秒后自来湖蓝化5min,切块脱水透明后蒸熟,树胶封片后拍照。随机选定3~5个视野,将同一视野的染色阴性细胞在显微镜明视野下计数,之后调至相差下对同一视野的所有细胞进行计数,两者之比即为神经元细胞的含量,同时估算阳性百分比。神经元细胞的形态学观察接种时细胞呈小球状,容积小,无瑕,彼此分散,难分辨细胞的形态结构。分散在培养板底,约6h后细胞开始贴壁,长出几微米凸起(图1)。约90上细胞在12h内贴壁,贴壁的神经元继续生长,凸出增多,伸长。2~4d后神经元凸出生长迅速,细胞之间开始产生网路;7d后,神经元细胞形态细腻,凸出多而粗大,细胞显著可辨,胞体呈方形或椭圆形,胞体较大,折光性好,光晕强,细胞交织成密集的神经元网络、突起狭长(图2)周后神经元细胞凸出逐步变细,细胞容积缩小,细胞开始死亡(图3)免疫细胞物理染色及含量测定NSE免疫细胞物理染色结果显示,染色大部份为阴性,染色呈深红色(图4)。
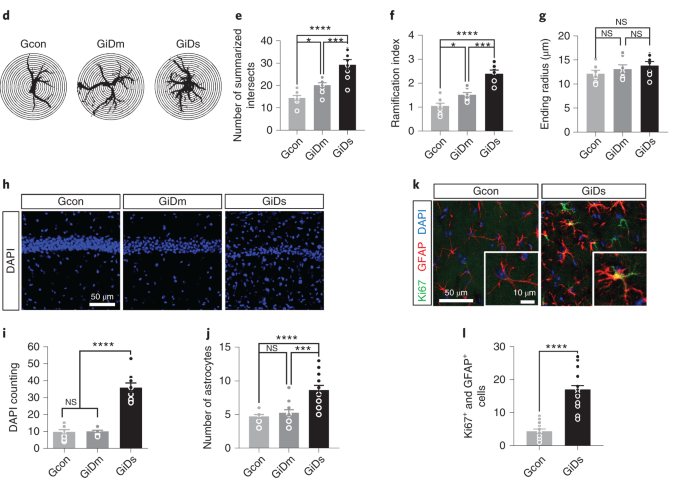
含量监测结果显示,培养7d后神经元细胞的含量可达90%左右。培养6h之后(200)免疫细胞物理染色(100)讨论背根神经节(DRG)主要为周围神经系统觉得神经元,培养DRG神经元可用于多种研究。往年培养多采用新生幼鼠,由于胚胎时期的神经元属较幼稚的阶段,较成年家兔便于成活,所以本实验采用胎鼠DRG神经元细胞培养方式的构建SD胚鼠,经观察培养发觉E16d的胚鼠DRG取材收获细胞多,神经元的分化能力强。影响神经元分离培养的诱因好多,取材的多少是培养的关键一步,本实验取材时取出脊椎后采用横剖和纵剖两种方式,结果发觉纵剖收获的神经元要显著少于横剖,这是由DRG特殊的解剖结构决定。消化是培养的另一关键诱因,胰酶是培养细胞时常用的消化酶,它在4时有微弱的消化作用,在37时消化作用强,EDTA主要汲取组织中的Ca。DRG神经元培养时常常都单一采用胰酶消化,本实验采用胰酶和EDTA的混和消化液进行消化,并且先在4冰柜中先让其充分作用20miCO2培养箱中消化20min,因为胚鼠的DRG比较软,加用EDTA,收到良好疗效。许多实验中常用神经生长因子(,NGF)和胶质源性神经生长因子(ophicGDNF)维持DRG神经元的体外存活,并促其凸出生长胞仍可以存活1个月左右,只要培养基中加入一定量血浆,完全可以毋须加入高昂的神经营养因子,这样可以大大减少研究成本,经济便宜。
另外,本实验的早期培养时加用过一定量药物,发觉小剂量的药物起不到抗菌作用,大剂量加入以后会影响细胞的生存,后期彻底不用时细胞生长挺好,所以本人不主张使用药物。本实验采用E16,取出脊椎后纵行解剖,用消化消化,不加用任何神经营养因子和药物,实验结果表明,神经元细胞生长状态良好,含量高,为进一步对神经元细胞的深入研究提供了经济、简单的实验模型。参考文献:植物细胞培养2基本技术掼[M].上海:科学出版社,2004.,1996,45:129.组织培养技术及其在医学研究中的应用[M].上海:中国协和医科学院出版社,2004:.,jiāHC,etal.2001,888,etal.lin2tedafternerve000,20,E,etal,1999,13(6):4302440.Root1,2