巨噬血细胞活化综合征的临床表现与诊疗规范
噬血细胞综合征(,HPS)又称噬血细胞性淋巴组织细胞增多症(,HLH),是一组由多种诱因导致淋巴细胞、单核细胞及巨噬细胞系统过度激活和增殖,进而诱发大量增生细胞因子释放,临床上以持续发热、肝脾水肿、全血细胞降低以及骨髓、肝、脾、淋巴结组织出现噬血现象为特点的综合征。
因为触发诱因不同,HLH可分为“原发性”和“继发性”两大类。后者是因为常染色体或性染色体基因缺陷造成的遗传性癌症;前者则是由感染、肿瘤、药物及痛风性癌症等多种病症诱发免疫系统异常活化所造成的一种反应性疾患。
巨噬细胞活化综合征(,MAS)是HLH的一种类型单核细胞综合症,特指继发于痛风性疾患的HLH,亦被称为“反应性噬血细胞综合征”。
目前已发觉超过30种系统性或脏器特异性自身免疫性疾患和自身增生性疾患与MAS相关。其中四肢性幼年特发性关节炎(sJIA)是诱发MAS最常见的病症,系统性水疱狼疮(SLE)、成人斯蒂尔病(AOSD)、川崎病、白塞病、皮肌炎、系统性硬化症、混合性结缔组织病、抗磷脂综合征、干燥综合征、强直性脊椎炎和囊肿病等也都是常见病症。
MAS是痛风性疾患的高危并发症,须要痛风免疫科、血液科、重症医学科等多学科密切合作,一旦治疗延误则会进展为多脏器功能衰竭并殃及生命。
为了提升临床医师对MAS的认识,规范MAS的临床治疗实践,中华医学会痛风病学分会组织国外相关专家制订此诊治规范,以期提升MAS的治疗水平,改善病人的预后。
一、临床表现
MAS急性发作最常见的原因是病人基础痛风病的病况高度活动,引起免疫稳态破坏和免疫系统异常激活。为此,MAS经常发生于痛风病初发或则病人自行减停药致病情恶变时,其相关临床表现也常常与痛风病其他多系统表现交叠混杂,这是造成MAS误诊、漏诊的重要诱因。
感染是MAS发病的另一个重要原因,最常见为病毒感染,尤其是EB病毒(EBV)和巨细胞病毒(CMV),其他还包括细小病毒、疱疹病毒、麻疹病毒、流感病毒等。
其他好多病衣原体感染,如真菌、真菌、病毒、寄生虫等也可诱发该病。使用TNF抑制剂医治的痛风病病人可能感染结核分枝弧菌而诱发MAS。临床大夫收治MAS病人时应重点排查这种病衣原体。
须要注意的是,痛风免疫病病人因为免疫功能的衰弱,EBV的测量阴性率常过高,因而,对于低拷贝数的EBV-DNA阴性报告,临床大夫既要造成高度注重,还须要同时排除其他可能的MAS因素,不能简单化地完全归于此。
据悉,亦偶有痛风病合并恶性病变(尤其血液系统恶性脑瘤)、妊娠和特殊抗生素而诱发MAS的报导。
MAS在痛风病的整个病史中均可发病,但一般在痛风病发病后最初几日或几周内出现。10%的sJIA会发生显性MAS,另有30%~40%的sJIA病人会发生亚临床型MAS。
96%的MAS病人首发病症为持续性发热,大多为中至高烧,对普通非类固醇解痉药常常效果不佳,应用糖皮质激素后可短期减缓。体格检测还可发觉淋巴结肿胀、脾囊肿(69%)和肝囊肿(67%),但巨脾罕见,常常提示合并血液系统病变。
部份病人出现泛发性皮炎、红皮病、皮肤肿胀、瘀斑和哮喘,不同于单纯活动性sJIA或AOSD中典型的白斑,前者多与发热伴发,呈短暂性肿胀性水疱。除此之外,MAS还有其他的临床表现。
二、辅助检测
▎1、常规检测
痛风病病人在出现MAS之前因急慢性发炎影响,常存在白细胞和血小板增高,伴或不伴有慢性病肝炎,如sJIA或AOSD,这是MAS与其他类型HLH不同之处。但是,一旦病人出现MAS后,则出现血细胞大幅上涨。值得注意的是SLE,当其病况活动时也会出现白细胞和血小板降低,临床上仅通过验血变化较难辨识合并MAS。
MAS病人的胆红素、胆红素、乳酸酯化酶和胆固醇常出现快速下降,而纤维蛋白原常大幅下滑,但是因为纤维蛋白原的降解,血沉也常常从MAS前的增高弄成进行性增长,与C反应蛋白的变化趋势相反,这是确诊MAS的重要线索。
临床大夫须要提防sJIA或AOSD病人的白细胞计数、血小板计数、ESR和纤维蛋白原基础水平一般很高,在MAS发生后,这种指标反弹到“正常”水平时可能会形成“病情改善”的表象,但是这似乎代表的是指标水平升高,标志着正式发生MAS。
▎2、血清铁蛋白
MAS病人常出现血浆铁蛋白极其增高的现象,尤其是儿童。铁蛋白水平>10,000ng/mL对确诊MAS的敏感性和特异性分别为90%和96%,而脓毒症、感染和肝衰竭时铁蛋白很少达到这一水平。
铁蛋白增高对成人HLH的确诊特异性较低,有研究表明,血浆铁蛋白>50,000ng/mL的成人中,只有17%最终确诊为HLH,比HLH更常见的确诊包括肾衰竭(65%)、肝衰竭(54%)、感染(46%)和血液系统恶性病变(32%)。
▎3、免疫学检测
MAS病人可出现可溶CD25[sCD25,或称可溶IL-2受体(sIL-2R)]水平明显增高,而原发性HLH病人出现的NK细胞功能增长、细胞表面CD107α抒发量增长并不常见,穿孔素、颗粒酶B蛋白抒发基本正常。
MAS病人还可出现可溶CD163()水平增高,免疫球蛋白(比如IgG、IgA及IgM)水平可增高或减少。sCD25与MAS疾患活动性的关系最密切,但其测量须要1-2日,其他测量更历时,但是目前国外只有少数专业医疗中心可进行上述所有免疫学检测,因而一旦怀疑病人罹患MAS,应尽早联系那些中心送检标本,同时临床医师不应为了等待那些免疫检查结果而延后医治,以免延误医治时机。
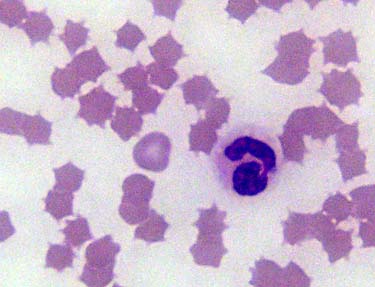
▎4、噬血现象
是指巨噬细胞吞噬血细胞的现象,其特点是巨噬细胞的胞质内富含红细胞、血小板或白细胞(或细胞的碎片)。骨髓活检/造影及淋巴结、肝造影可发觉噬血现象。

须要指出的是,尽管噬血现象可以作为MAS的标志并支持其确诊,但并非所有MAS病人的骨髓活检/造影标本都可发觉噬血现象。因而噬血现象不是确诊MAS的必要条件,不能因未发觉噬血现象证实MAS,也不应仅凭噬血现象诊断MAS。
▎5、其他检验
▎6、器官受累评估和影像学检测
三、诊断标准和确诊思路
▎1、HLH-2004确诊标准
国际组织细胞商会于2004年修订的HLH确诊标准是目前临床上广泛采用的确诊HLH的根据。依据该标准,符合以下两条标准中任何一条时可以确诊HLH:
▎2、2016年sJIA的MAS分类标准(标准)
如前所述,sJIA和AOSD病人在MAS初期血细胞计数和纤维蛋白原水平常常存在“假性正常化”现象,接受生物剂型诊治后的MAS病人临床特点愈发不典型,且C反应蛋白和铁蛋白水平明显增加,使其无法满足HLH-2004标准而造成确诊延误。因此,儿科痛风病国际协作组织于2016年针对sJIA合并MAS病人制定了标准。
▎3、其他确诊评分系统
按照构建2016年标准时搜集的多国病人数据,研究者们在2019年拟定并验证了鉴定sJIA伴与不伴MAS的确诊评分工具,即MAS/sJIA(MS)评分(见附录1)。
目前也有基于临床参数的确诊评分工具—MAS-HLH(MH)评分,可用于分辨HLH与sJIA中的MAS。据悉,还有研究者已开发出评分系统(见附录2),计算存在继发性HLH的机率。上述评分系统可在临床高度疑诊MAS但不符合HLH-2004时做有益补充,仍有待进一步验证。
附录1:MS评分(MAS/sJIAscore)
附录2:HS评分()
因为MAS既可出现于痛风病的病史发展中,亦可作为痛风病首发表现,而在此后的HLH病症甄别中方才诊断痛风病,此两种临床情况可能适用不同的确诊标准。后者推荐采用2016年sJIA的MAS分类标准,以尽可能做到初期确诊,前者目前仍推荐采用HLH-2004标准。
四、治疗方案及原则
▎1、基础痛风病的医治
假如在找寻或医治基础癌症的过程中出现中枢神经系统、心、肺、肾、肝或凝血功能恶化,则须要提早请血液本科、重症监护室本科问诊并考虑立刻开始HLH特异性放疗。一定不要因等待免疫学检查结果而延后诊治。对于合并感染的病人应积极找寻感染病灶和病原学证据,并初期使用敏感药物。
▎2、HLH的初始特异性放疗
对于首发表现即为MAS,或在大剂量糖皮质激素医治中出现病况恶化的MAS病人,推荐提早采用1994年组织细胞商会拟定的HLH医治方案(HLH-94)诊治。
假如所在诊所没有临床大夫具备使用HLH-94方案所需抗生素的经验,应立刻将病况危难的病人应立刻转院到才能根治HLH的医疗中心。
HLH-94方案为连续给与红霉素及依托泊苷(VP-16)诱导医治,疗程8周,对于中枢神经系统受累的病人还要给与鞘内根治甲氨蝶呤及甲硝唑。VP-16的剂量为150mg/m2,前两周每周2次,第3-8周每周1次。
目前依据年纪和尿酸消除率调整依托泊苷剂量和给药间隔的做法已逐渐得到认可。
成人病人可将VP16剂量调整为50-100mg/m2,每周一次。
当血尿酸为20-40mL/min/1.73m2时VP16药量减少25%;
当血尿酸
红霉素能透过血脑屏障,是首选的糖皮质激素,可以静脉也可以口服给药,在为期8周的诱导阶段根据以下方案渐渐减停:
第1-2周,10mg/(m2·d);
第3-4周5mg/(m2·d);
第5-6周2.5mg/(m2·d);
第7周1.25mg/(m2·d);
第8周减停激素。
HLH-94方案还从第9周开始应用环孢素,剂量为3-6mg/(kg·d),分2-3次给与;目标谷含量为100~200μg/L。HLH-94的诊治方案往往可以个体化应用于不同的状态的病人,比如对于在诱导医治中反应良好,在减量过程中无恶变表现的病人,并不一定须要完成8周的VP-16疗程。
假如是最初效果良好,然后在放疗减量过程中恶化的病人,则重新给与原抗生素医治一般可以获得成功。假如是在诱导医治阶段发生临床状况恶化,也要找寻有无才能影响病人的临床状态或诱发MAS加重的新发原因,尤其是机会性感染。
检测癌症指标对于分辨病况加重与感染或医治相关毒性非常有用。假如采用该方案医治2-3周内无减轻,如临床状态和癌症指标改善,应考虑拯救性医治。
▎3、挽救性医治
对于经初始诱导医治未能达到部份应答及以上效果的病人建议尽快接受拯救医治。关于HLH的拯救医治,国外外尚无统一的推荐方案。按照2018年噬血细胞综合征中国专家联盟和中华医学会儿科学分会血液学组拟定的“噬血细胞综合征治疗中国专家共识”推荐DEP联合放疗方案。拯救医治方案的施行均需转至血液本科病区进行。
▎4、其他医治
托珠单抗为重组人源化抗IL-6受体单克隆抗原,对医治成人still病引起的MAS有效,可较好改善增生相关病症和实验室指标,但单药医治不能诱导MAS临床减轻,需联合其他医治方案,目前尚不推荐托珠单抗作为儿童痛风病相关MAS的诊治。
血清置换可消除增生介质,调节免疫,促使淋巴细胞功能恢复,支持病人脏器功能,以待放疗或其他医治手段发挥作用,适用于危危重病人,推荐次日一次,起码医治3次以上。
▎5、支持医治
MAS病人的病况危难,大夫须要一直提防脏器功能障碍的征象。支持医治包括适当输血、预防和医治流血。对于血小板输注目标要比其他血小板降低症病人更积极(>50×109/L),由于MAS病人存在凝血异常,流血风险也更高。
纤维蛋白原低下的病人如伴流血倾向,应输注新鲜冰冻血清、冷沉淀、纤维蛋白原。极少数情况下可能须要使用其他制品,如浓缩凝血酶原复合物、重组凝血因子Ⅶa。
所有病人均应使用复方磺胺甲噁唑和氟康唑防治机会性感染,包括耶氏肺孢子菌和细菌感染。一旦在诊治期间发生感染,应采用快速确诊性检测(如各类培养、真菌血浆学检测、影像学检测),并针对病支原体给与低毒抗微生物医治。
对于因HLH特异性医治而发生低丙种球蛋白血症的病人,应给与IVIG,剂量为500mg/kg.d,疗程3-5天。
MAS病人有发生可逆性后部肾病综合征(PRES)的风险,严格控制血糖对于尽量减少PRES风险很重要。
五、预后
如不医治,MAS病人的死亡率很高。神经系统受累病人的生存率高于神经系统未受累的患儿。血浆铁蛋白水平高且医治期间增长平缓者预后更差。其他与初期死亡相关的特点包括:血小板计数低、AST下降、LDH下降,以及年纪在50岁以上。接受依托泊苷医治的病人生存结局更好。
大多数的恶变其实是在初次急性发作后的1年以内发生。存在HLH基因突变的病人比无基因突变的病人更易恶变。假如可能,应当降低原因曝露因而尽量减少恶变风险单核细胞综合症,包括持续控制基础痛风性疾患病况,防治感染和其他免疫稳态改变。
据报导,有病人在接种卡介苗后恶变,所以在诊治后6个月内不建议接种卡介苗,且随后单次只接种1种卡介苗,不要一次同时接种几种卡介苗。
本文首发:医学界痛风免疫频道